سنگهای قیمتی، گوهر شناسی و سنگ شناسی
هالیت آبی (Blue Halite): از خواص سنگ نمک آبی تا علت رنگ آن
هالیت (Halite) نام یک کانی تشکیل شده از سدیم کلرید (NaCl) و ماده ای است که عموما آن را به عنوان سنگ نمک می شناسند. هالیت غالباً در سنگهای رسوبی که از تبخیر آب دریا یا آب دریاچه شور به وجود آمده است، وجود دارد. این کانی معدنی معمولاً بی رنگ یا سفید است، اما بسته به اینکلوژنهای سایر مواد، ناخالصی ها و عیوب ساختاری یا ایزوتوپی در بلورها، ممکن است آبی روشن، آبی تیره، بنفش، صورتی، قرمز، نارنجی، زرد یا خاکستری نیز باشد.
فهرست مطالب
آیا نمک های رنگی مفیدند؟
در سال 2016، اداره فدرال ایمنی غذا و دامپزشکی سوئیس (FSVO) مطالعه گسترده ای را روی 25 نوع مختلف نمک از سراسر جهان انجام داد. ایوا ون بیک، کارمند روابط عمومی FSVO، توضیح میدهد: «این اولین باری بود که این نوع مواد غذایی را بررسی میکردیم.» اکنون چنین انواع نمک در مغازههای بیشتری یافت میشود و اغلب بهعنوان بسیار طبیعی و برای سلامتی مفید معرفی میشوند، در حالی که ما در مورد ترکیب شیمیایی آنها اطلاعات کمی داریم.

نتایج منتشر شده در ماه مه 2016 نشان میدهد که انواع نمکهای غیر رایج، در کل، کمتر از نمک معمولی «سالم» هستند، زیرا حاوی ید کمتری هستند. نمک رنگی تنها حاوی 94 درصد کلرید سدیم هستند، در مقایسه با 99 درصد نمک خوراکی معمولی، به این معنی که حاوی عناصر دیگری هستند. آلومینیوم، اورانیوم و کادمیوم از جمله آلایندههایی هستند که در نمک رنگی یافت میشوند، اگرچه در مقادیر “بسیار کم” برای سلامتی .

جالب است بدانید نمک هیمالیا حاوی مقادیر قابل توجهی آهن است که رنگ صورتی آن را توجیه می کند. با این حال، به شکل اکسید آهن نامحلول است، بنابراین جذب این ماده معدنی برای بدن دشوار است. در نتیجه، FSVO معتقد است که نمک هیمالیا را نمی توان به عنوان منبع تغذیه ای خوب آهن در نظر گرفت. Codex Alimentarius و فائو (FAO) و سازمان بهداشت جهانی (WHO)، دستور العمل هایی شامل استانداردها و مراجع مربوط به درجه کیفیت نمک از نظر غذایی تحت عنوان «ترکیبات ضروری و فاکتورهای کیفی»، این سند تصریح میکند که محتوای کلرید سدیم نمک غذایی «نباید کمتر از 97 درصد بر اساس ماده خشک، بدون افزودنیها باشد». محتوای کلرید سدیم در برخی از انواع نمک های غیر رایج تنها 94٪ یا حتی در برخی موارد به 88٪ نیز می رسد.
آیا نمک آبی خواص بالاتری نسبت به نمک های رایج دارد؟


اما مورد بعد در مورد نمک های آبی این است که آنها رادیواکتیو نیستند. شایعاتی درباره پرتوهای گامای ناشی از پتاسیم-40 ناشی از سیلویت مطرح شده که با توجه به تحقیقات من معنا و مفهومی ندارد. درواقع K40 بسیار کم رادیواکتیو بوده و جالب است بدانید که حتی موز به دلیل پتاسیم ، اندکی رادیواکتیو است ولی هیچ ضرری برای بدن ندارد. میزان رادیواکتیوته نمک آبی حتی از موز هم کمتر است. این شایعات در برخی مجامع زمین شناسی ایران به قدری جدی بود که یکی از پیج های اینستاگرام معروف فروش سنک نمک آبی ، جهت اثبات روی به اندازه گیری میزان پرتو گاما آورده بود! .
علت رنگ هالیت آبی

اگرچه علت رنگهای آبی و ارغوانی که در هالیت های کارلسبد در نیومکزیکو و سایر مکانهای سراسر جهان مانند کویر سمنان ایران دیده میشود، کاملاً شناخته نشدهاند، با این حال نتایج معقولی را میتوان از مطالعات در چندین نشریه و مشاهدات میدانی گرفت. دو پدیده مشاهده شده که بخشی از فرآیندی ایجاد سایهرنگ های متفاوت آبی و ارغوانی را ایجاد میکنند، وجود دارد (شکل 1 و 2).

به طور معمول هالیت آبی و ارغوانی (تا بنفش) در تماس مستقیم با سیلویت نسبتاً خالص (که معمولاً سفید شیری است) رخ می دهد. سیلویت (KCl) حاوی مقدار کمی از ایزوتوپ طبیعی رادیواکتیو پتاسیم-40 (K40) است که به آرامی در طول زمان واپاشی شده و ذرات بتا و تابش اشعه گاما را آزاد می کند. این تابش همان مقدار بسیار کمی از تشعشعات است که حتی با خوردن موز نیز بدن ما در معرض آن قرار می گیرد، بنابراین برای انسان مضر نیست. جالب است بدانید رنگ نمک آبی با حرارت دهی نیز میتواند تغییراتی داشته باشد.

در ابتدا، پرتوهای گاما حاصل از واپاشی 40K یک الکترون را از یونهای کلر (Cl-) که در ساختار کریستالی هالیت معلق هستند جدا میکند و الکترونهای آزاد (-) و کلر عنصری (Cl) تولید میکند. الکترونها به سمت مکانهای اتمهای از دست رفته (فضای خالی) حرکت میکنند و یک نقص بسیار ریز ساختاری در ساختار بلوری به نام مرکز فارب (Farbe-center) تشکیل میدهند («Farbe» در آلمانی به معنای رنگ است، بنابراین به آنها مرکز رنگ (color-centers) نیز میگویند). الکترون ها در چنین فضای خالی تمایل به جذب نور در طیف مرئی دارند به طوری که ماده ای که معمولاً شفاف است رنگی می شود.
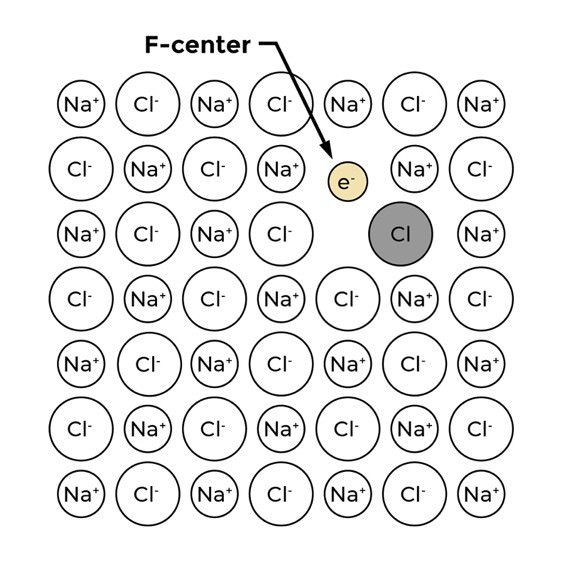
در بحث نمک آبی ، نقص ایجاد شده توسط مرکز رنگی F (F-center) بر نحوه عبوری/انعکاسی پرتو نور از یک قسمت ماده تأثیر میگذارد که باعث ایجاد رنگ قابل مشاهده در طیف مرئی برای ما میشود. در این حالت، مرکز رنگی F یک رنگ زرد تا قهوه ای در هالیت ایجاد می کند (شکل 3). ثانیاً، برخی از الکترونهای آزاد با یونهای سدیم باردار شده مثبت (Na+) ترکیب میشوند تا سدیم عنصری (Na) تولید کنند. اتم های عنصری فلز سدیم به یکدیگر جذب می شوند تا گروه ها یا کلوئیدها را تشکیل دهند که رنگ آبی را در هالیت ایجاد می کند. اشباع رنگ به قرار گرفتن در معرض تشعشع مربوط می شود، بنابراین هالیت تیره رنگ یا در معرض دوزهای بالاتر تشعشع (نزدیک به سیلویت) قرار داشته یا برای مدت طولانی تری در معرض تابش قرار گرفته است (شکل 4).

فیل و مشاور فارغ التحصیل او، دکتر ویرجیل لوث، برای آزمایش تأثیر تابش UV بر روی مرکز رنگی F در هالیت آبی کارلس بد، مجموعه ای از آزمایشات را ابداع کردند که هالیت را در معرض یک نور فرابنفش موج کوتاه پرقدرت قرار می دهد. مانند بسیاری از مواد معدنی که توسط F-center می شوند، تابش UV الکترون به دام افتاده را از جای خالی مرکز رنگی F خارج می کند و رنگ اصلی کانی را به قبل از تابش باز می گرداند. یک فرآیند مشابه که بسیاری از مردم محلی با آن آشنا هستند در رابطه با فلوریت آبی از بلانچارد، نیومکزیکو است. بیشتر فلوریتهایی که در آنجا وجود دارند، رنگ آبی متوسط تا تیره خوبی دارند، اما هنگامی که در معرض نور طبیعی UV خورشید قرار میگیرند، کریستالها سفید تا بیرنگ یا سفید شوند، که رنگ اصلی فلوریت در زمان تشکیل آن می باشد. فیل و دکتر لوث فرض کردند که هالیت به شیوه ای مشابه رفتار خواهد کرد. نتیجه نهایی این است که ارغوانی با بازیابی نقص ساختاری اولیه زرد/قهوه ای، ناپدید می شود، در حالی که آبی از بین نمیرود زیرا کلوئیدهای سدیم عنصری همچنان باقی می مانند. همانطور که انتظار می رفت پس از انجام آزمایشات به مدت 48 ساعت، تغییر محسوسی مشاهده شد. رنگ ارغوانی هالیت محو شده بود و یک هالیت آبی خالص باقی ماند. فرضیه درست بود! (شکل 5).

بسترهای پتاس در منطقه کارلسبد گسترده است و می توان انتظار داشت که هالیت های آبی در همه جا در تماس با سیلویت وجود داشته باشد. با این حال، بیشتر سیلویت های آن منطقه قرمز هستند که رنگشان ناشی از هماتیت است. چند مکان در معادن وجود دارد که سیلویت دچار انحلال و تبلور مجدد شده و هماتیت را از بین می برد و در واقع آن را تصفیه می کند. در جایی که هماتیت در سیلویت وجود دارد، به عنوان یک بازدارنده عمل می کند و تابش طبیعی پتاسیم-40 را مسدود می کند. بنابراین، بیشتر سنگ نمک های هالیت در بسترهای پتاس بی رنگ می ماند یا توسط اکسیدهای آهن به رنگ نارنجی در می آید. ته رنگ های هالیت ارغوانی تا آبی نتیجه ترکیب مراکز رنگی F و سدیم کلوئیدی با میزان شدت متفاوت است (شکل 6). هالیت ارغوانی شامل ترکیبی از هر دو پدیده است، در حالی که هالیت آبی نشان دهنده کمبود مراکز رنگی F موجود در کریستال یا ناحیه خاصی از کریستال است. تک بلورها در طول بیش از دو متر مشاهده شدهاند و در ناحیهای به این بزرگی، بسیاری از سایههای بنفش و آبی میتوانند در یک بلور وجود داشته باشند (شکل 7). این ویژگی در بلورهای هالیت سمنان نیز قابل مشاهده است.

شکل 7. عکسی از دو کریستال بزرگ هالیت بیش از یک متر که توسط سیلویت با خلوص بالا محصور شده اند. هالیت در طول زمان زمین شناسی در معرض تشعشعات یونیزه کننده قرار گرفته است. رنگ قهوه ای اولین رنگ در معرض تابش است. آبی و ارغوانی نشان می دهد که هالیت در معرض تشعشعات طولانی تر/ قوی تری قرار گرفته است. بلورهای بزرگی مانند این اغلب حاوی هستههای کهربایی رنگ هستند، که نشان میدهد سدیم کلوئیدی تمایل به تجمع در نزدیکی سطح تماس با سیلویت دارد.
هندسه و توزیع رنگ هالیت آبی
هندسه توزیع رنگ یکی دیگر از جنبه های جالب هالیت ها در سایر مناطق در سراسر جهان از جمله سمنان و نیومکزیکو است و مکانیسم های رنگینگی آنها بسیار کم شناخته شده اند. در مطالعات که تا کنون انجام شده تلاش شده تا توضیح دهند که چه چیزی باعث ایجاد رنگ در سطح اتمی می شود، اما به دلیل ماهیت ناپایدار هالیت در هنگام قرار گرفتن در معرض تکنیک های تحلیلی پیشرفته، تا حد زیادی ناموفق بوده اند. به عنوان مثال، هالیت در معرض یک پرتو الکترونی (توسط ابزار میکروپروپ الکترونی)، به سادگی تبخیر می شود . با این حال، اگرچه کالر زونینگ اندکی وجود دارند که میتوانیم بر اساس کریستالوگرافی و سریهای محلول جامد حدس بزنیم، اما سایر توزیع رنگها هنگام تلاش برای تشخیص آنچه اتفاق میافتد بسیار مشکلسازتر هستند. منطقه بندی رنگی اغلب در نوارها (یا مناطق) که در امتداد صفحات رشد کوبیک و گاهی اوقات هشت وجهی) کریستال های هالیت رخ می دهد، تشکیل می شود. این پدیده ممکن است توضیح نسبتاً سادهای داشته باشد: کریستالوگرافی ، کالر زونینگ (منطقه بندی رنگی) را بر اساس وجود یک سری محلول جامد بین هالیت و سیلویت کنترل میکند. به ندرت در طبیعت یک عضو نهایی ماده معدنی یا بلور خالص بدست می آوریم. آنچه ما اغلب می بینیم تغییرات ترکیبی (سری محلول جامد)، به دلیل جایگزینی یک یون معین به جای یون دیگری در کانی هایی است که همساختار با همان فرمول شیمیایی پایه هستند. کانی های معدنی مانند وانادینیت (Pb5(VO4)3Cl) و میمتیت (Pb5(AsO4)3Cl) یا هالیت (NaCl) و سیلویت (KCl) اغلب در صورت وجود عناصر مربوطه با هم متبلور می شوند و در بسیاری از موارد آنها یک عضو واسطه را تشکیل می دهند که هر دو عنصر در یک کریستال را دربر می گیرند.

در مورد هالیت کارلسبد، انحلال/ رسوب مجدد گسترده (ترازایش) منجر به متبلور شدن محلول های نمکی غنی از پتاسیم و سدیم به هالیت می شود که همچنین مقداری پتاسیم را در شبکه بلوری خود گنجانده اند. به دلیل ساختار کریستالی هالیت و سیلویت (ایزومتریک)، پتاسیم اغلب در امتداد وجههای کوبیک در حال گسترش جذب میشود. اینکه آیا این یون های پتاسیم بود یا سیلویت هنوز مشخص نیست. این جایگزینی محلول جامد بین Na و K منجر به نواحی متناوب رنگی و بی رنگ در امتداد صفحات کریستالی می شود (شکل 8 و 9).

توضیح علت هندسه های دیگر بسیار دشوارتر است. گاهی اوقات رنگ می تواند در “حباب های” بی شکلی که کنترل ساختاری قابل تشخیصی ندارند وجود داشته باشد (شکل 10). اینجا چه اتفاقی افتاد؟ آیا بعد از متبلور شدن هالیت، قسمتی از انحلال وجود داشت؟ آیا غلظتی از پتاسیم وجود داشت که در امتداد صفحات کریستالی قرار نگرفته؟ برخی از آزمایشات نشان داده است که هالیت آبی محلول شده یا با استرس زیاد ، رنگ خود را حفظ نمی کند.


آیا فشار لیتواستاتیک عاملی در این نوع هندسه است؟ شکاف ها، حتی در صورت تبلور مجدد، اغلب در میان هالیت رنگی بی رنگ هستند (شکل 11).


حتی شرح ماجرا زمانی سخت تر می شود که بخواهیم درباره چیزی که آن را “میلههای رنگ” می نامیم، سخن بگوییم. اینها ظاهر لوله های رنگی دارند که می توانند چندین سانتی متر طول عمود بر سطح کریستال داشته باشند که توسط هالیت بی رنگ احاطه شده اند (شکل 12 و 13).

شاید گیجکنندهترین هندسهها رنگهایی باشند که به صورت “رگه های حلقه ای” عموماً در یک جهت شروع میشوند، اما زمانی که در مقیاس کوچکتر مشاهده میشوند مسیرشان را بهطور تصادفی تغییر میدهند یا اصلاً الگوی قابل تشخیصی ندارند (شکل 14 و 15).

چه چیزی این هندسه ها را کنترل می کند؟ پاسخ به این سؤالات بر اساس مشاهده در سطح کلان واضح نیست، اما زمانی که در سطح اتمی مورد بررسی قرار گیرد، میتواند آشکارتر شود. اگر فناوری به حدی پیشرفت کند که پرتو الکترونی تنها ابزاری برای بررسی ساختار و ترکیب اتمی در کانیشناسی نباشد، این یک حوزه مطالعه جالب برای پایاننامه خواهد بود.
منابع:
special thanks of Philip Simmons Copyright Phillip Simmons 2021 youngmineralcollectors.orgphotography :Jeff ScovilINFANGER, Esther et HALDIMANN, Max, 05.2016. Bickham, M. 2012. Chemical analysis of blue halite. Geological Society of America, Abstracts and Programs, 44 (1), 8. Klein, Cornelis. 2002. The Manual of Mineral Science, 22 nd ed. New York: John Wiley & Sons, Inc. 641p. Simmons, Philip. 2013. The Carlsbad Potash Basin, Carlsbad, New Mexico. Mineralogical Record 44 (1), 13-49. Sonnenfeld, P. 1995. The color of rock salt – a review. Sedimentary Geology, 94, 267-276.

